Adenoviridae
 צמד אדנו וירוסים מבעד למיקרוסקופ אלקטרוני סורק
צמד אדנו וירוסים מבעד למיקרוסקופ אלקטרוני סורק
| |
| מיון מדעי | |
| קבוצה: | קבוצה I (נגיפי dsDNA) |
| משפחה: | Adenoviridae |
| סוגים | |
| |
Adenoviridae (בעברית: נגיפי אדנו[1]) היא משפחה של נגיפי DNA דו-גדילי, חסרי מעטפת ("ערומים"), בגודל של 90–120 ננומטר, המכילים קפסיד איקוסהידרלי, בעלי תפוצה עולמית.
משפחת ה-Adenoviridae מורכבת מחמישה סוגים של הנגיף, להם פונדקאים רבים בעולם החי: Atadenovirus - (עופות, זוחלים ויונקים), Aviadenovirus - (עופות), Ichtadenovirus - (דגים), Siadenovirus - (דו-חיים ועופות), Mastadenovirus - (יונקים).
הסוג Mastadenovirus, אשר כמעט באופן בלעדי גורם למחלות בבני האדם, מכיל 57 זנים של אדנו וירוסים. וירוסים אלה גורמים למגוון רחב של מחלות, החל מהצטננויות קלות בדרכי הנשימה וכלה במחלות ויראליות מסכנות חיים כמו דלקת ריאות, וזיהומים ויראליים בעיניים ובמערכת העיכול בילדים ובמבוגרים כאחד.
משפחת ה-Adenoviridae התגלתה לראשונה בשנת 1953, כאשר החוקרים הבחינו בניוון של תרבית אדנואידית (מרקמת שקד האף), ולא יכלו לייחס זאת לשום פתוגן ידוע, ומכאן מקור שמה.

מבנה
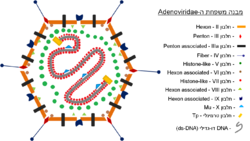
נגיפי משפחת ה-Adenoviridae, הם נגיפים חסרי מעטפת נגיפית ("ערומים"), בגודל של 90–120 ננומטר, המכילים קפסיד איקוסהידרלי. נגיפי המשפחה מכילים גנום DNA דו-גדילי בעל 35–36 אלף בסיסים[2], פרט לנגיפים מהסוג Atadenovirus בעלי 30 אלף בסיסים. DNA זה מקודד לכ-20 עד 40 חלבונים שונים (מספר החלבונים משתנה בהתאם לסוג הנגיף). הגנום ארוז, יחד עם מספר חלבוני ליבה, בתוך מעטפת חלבונית קשיחה, הקרויה קפסיד. צורתו של הקפסיד היא איקוסהידרלי, והוא מורכב מ-252 תת-יחידות:
- 240 חלבונים מסוג Hexon (קרוי גם חלבון II).
- 12 חלבונים מסוג Penton (קרוי גם חלבון III).
לכל Penton צמוד, בעודו פונה כלפי חוץ, חלבון מסוג Fiber (קרוי גם חלבון IV), המשמש את הנגיפים להכרת רצפטורים ספציפיים על גבי התאים, שאליהם הם חודרים. נוכחות חלבוני ה-Fiber מקנים לווירוסים במשפחה צורה של מעין לווין.
חלבונים מבניים נוספים, המהווים חלק מתוך הקפסיד הוויראלי הם: חלבון VI וחלבון VIII (קרואים גם Hexon associated proteins) המצויים בחלקו הפנימי של הקפסיד, חלבון IIIa (קרוי גם Penton associated protein) החוצה את הקפסיד וחלבון IX, המצוי בחלקו החיצוני של הקפסיד.
לחלבוני הליבה של הנגיפים תפקידים בשמירת התקינות והשלמות של המטען הגנטי:
- חלבון V, חלבון VII[3] וחלבון X (הקרוי גם Mu) - חלבונים דמויי היסטונים (Histone-like proteins), אשר תפקידם העיקרי הוא לעטוף את הגנום הנגיפי ולשמור עליו בפני נזקים פיזיים וכן בפני מנגנונים אנטי-ויראליים בתוך התא, אשר מסוגלים לגרום לפירוק ה-DNA הנגיפי ו/או לאיחוי ה-DNA הנגיפי למולקולת DNA אחת ארוכה, המורכבת ממספר רב של יחידות DNA נגיפיות זהות, בשם קונקטמר (Concatemer).
- חלבון טרמינלי (Terminal protein, בקיצור: TP) - חלבון שנמצא בשני קצוות הגנום, על גבי גדיל 5'. מטרתו היא לגייס את האנזים הנגיפי DNA פולימראז לאחר תחילת שכפול ה-DNA.
הדבקה ומחזור התרבות
מחזור החיים של הנגיפים במשפחה מחולק לשלושה שלבים, בדומה למרבית הנגיפים הידועים: שלב מוקדם, שלב ביניים ושלב מאוחר. השלב המוקדם מתאפיין באינטראקציה של הווירוס עם הרצפטור על פני ממברנת התא, בחדירה, בשעתוק ובתרגום של הגנים הוויראליים המוקדמים. שלב הביניים מתאפיין בשכפול הגנום הוויראלי ואילו השלב המאוחר מתאפיין בשעתוק וסינתזה של חלבונים מבניים, אריזת ויריונים, הרג התא המאכסן ושחרור הווירוסים החדשים אל מחוץ לתא המאכסן.
להלן תיאור מחזור ההדבקה וההתרבות בנגיפי Adenoviridae המדביקים חולייתנים ממחלקת היונקים.
שלב מוקדם
חדירה לתא המאכסן והמעבר לגרעין
לאחר היצמדות נגיפי האדנו אל תאי האפיתל של מערכת הנשימה, באמצעות אינטראקציה של חלבוני ה-Fiber הנגיפיים עם חלבונים טראנסממברנליים מסוג CAR[4] (Coxsackievirus and adenovirus receptor), להם תפקיד חשוב בהצמדת תאים אחד לשני (Adhesion), או עם רצפטורים מסוג: CD86 ,CD80 ,CD46 (רק נגיפים מסוג Human adenovirus B), מתרחשת אינטראקציה משנית של חלבוני ה-Penton עם הקו-רצפטורים התאיים מסוג אינטגרין, בעלי שרשרות אלפא ובטא מסוג αVβ3 או αVβ5. אינטראקציה משנית זו מאפשרת למעשה את חדירת הנגיפים אל תוך התא בתהליך של אנדוציטוזה, המושרית על ידי חלבוני קלתרין. בשלב הבא, כתוצאה מהסביבה החומצית השוררת בתוך האנדוזום, עוברים הנגיפים שלב של השלת הקפסיד (Uncoating) וכך חושפים את תכולתם בציטוזול. חלבוני הליבה, אשר עוטפים את הגנום הנגיפי מכילים רצפים ייחודיים, המזוהים על ידי מנגנוני שינוע בתא, כרצפים המייעדים את החלבון להיכנס לתוך הגרעין. מנגנוני השינוע הללו, המתבססים על פעילות מיקרוטובולים וחלבוני עזר מוטוריים, דוגמת דינאינים, מחדירים את ה-DNA לתוך הגרעין דרך נקבוביות בקרומית הגרעין, כעבור שעתיים מרגע ההדבקה[5].
ביטוי הגנים המוקדמים

מיד עם חדירת ה-DNA הנגיפי לגרעין, מתחיל שעתוק של חמשת הגנים הוויראליים המוקדמים: E4, E3, E2, E1B, E1A באמצעות האנזים RNA פולימראז II תאי, וכן של מקטעי RNA קצרים, הקרויים VAI-RNA (Virus-associated RNA I) על ידי האנזים RNA פולימראז III תאי. חמשת הגנים המוקדמים משועתקים למספר רב של תוצרי mRNA על ידי שימוש בשחבור חליפי ופוליאדנילציה משתנה.
- E1A - הוא הגן הראשון המתבטא לאחר שהגנום הנגיפי מגיע אל גרעין התא המאכסן. הגן מקודד לשני חלבונים עיקריים (243R ו-289R), המשפעלים שעתוק, מורידים את סינתזת האינטרפרון הראשונית בתאים מודבקים[6] (עיקר ויסות התגובה החיסונית כלפי הדבקה אדנו ויראלית מתבצע על ידי חלבוני הגן E3) וגורמים לתא המאכסן להתקדם לשלב ה-S במחזור התא. המעבר לשלב ה-S מתאפשר על ידי דיכוי חלבון הרטינובלסטומה (pRB) - חלבון אשר מונע באופן טבעי מהתא להתקדם משלב G1 ל-S על ידי עיכוב גורם השעתוק E2F[7]. לתוצרי E1A תפקיד חשוב בשפעול שעתוק של גנים ויראליים ותאיים[8]. עם זאת, חלבוני E1A אינם כוללים רצף ספציפי של קישור ל-DNA. במקום זאת הם נקשרים לפקטורי שעתוק ולחלבונים רגולטוריים שונים, דוגמת פקטור השעתוק AP1 וכך מבקרים את מידת השעתוק של הגנים השונים. פעילותו של E1A מעודדת, בסופו של הדבר, גם את השריית המוות המתוכנן של התא המאכסן, כלומר אפופטוזה. ביטוי של גנים מוקדמים נוספים של הנגיף עוזר לו להתמודד עם הבעיה ולהחזיק את התא המאכסן בחיים.
- E1B - הוא הגן שמקודד לשני חלבונים מעכבי אפופטוזה, שפעילותם מונעת את הפעלת המסלולים האפופטוטיים המושרים על ידי E1A. החלבון הראשון, E1B-19kDa, מהווה הומולוג של החלבון התאי Bcl-2[9], הידוע כמעכב אפופטוזה ומונע בכך מוות בטרם עת של התא המאכסן, שעלול לפגוע ביעילות יצור הוויריונים. החלבון שני, E1B-55kDa, נקשר לחלבון מדכא הגידולים p53 ומונע ממנו לגרום לעצירה בשלב G1 של מחזור התא. E1B-55kDa, ביחד עם חלבון ויראלי נוסף (E4orf6), מעודד פירוק של חלבונים תאיים, המעורבים בהפעלת תגובה לתיקון נזקי DNA, הנגרמת בעקבות יצור מוגבר של DNA דו-גדילי זר בתוך התא המאכסן. בנוסף לכך, E1B-55kDa הוא בעל תפקיד קריטי בבקרת המעבר של mRNA ויראלי מתוך הגרעין לציטופלסמה[10].
- E2 - הוא הגן שמקודד לשני חלבונים הנחוצים לשכפול ה-DNA הנגיפי (E2A ו-E2B): ה-DNA הנגיפי מסונתז על ידי E2B DNA polymerase. ואילו חלבון E2A הוא פפטיד קטן במשקל 72kDa הקושר DNA חד-גדילי (הנוצר רגעית בתהליך הרפליקציה), על מנת להגן עליו בפני אנזימים תאיים שמטרתם לפרק DNA חד-גדילי, וכן מבקר שעתוק ותרגום גנים ויראליים בשלבים המאוחרים של ההדבקה[11].
- E3 - הוא הגן שאחראי על ויסות התגובה של המאכסן כלפי הדבקה אדנו ויראלית, ובכך מגן על התא המודבק מפני תגובה חיסונית של הגוף[12]. חלבונים המקודדים על ידי E3 משפיעים על תפקודם של קולטנים לאינטרפרון על פני ממברנת התא המאכסן ומבקרים מעבר אותות תוך תאי, על מנת לדכא הפרשה של פקטורים פרו-דלקתיים מהתא המודבק. כמו כן נמצא כי ביטוי החלבון E3-19kDa גורם לירידה בקולטנים מסוג MHC-1, דבר הגורם לירידה בפעילות הציטוטוקסית של תאי T ציטוטוקסיים[13].
- E4 - גן זה מקודד לשבעה חלבונים, הנוצרים כתוצאה משעתוק 6 מסגרות קריאה פתוחות ומשחבור חליפי של ה-RNA. לפיכך כל תוצרי הגן נושאים את השם E4 open reading frame 1-7 (בקיצור: E4orf1-7). שעתוק של יחידת E4 מבוקר על ידי פרומוטר בודד, אשר משופעל על ידי E1A והשליח השניוני cAMP[14], כשעתיים לאחר ההדבקה. בשלבים מאוחרים של ההדבקה מעוכב השעתוק של יחידה E4 הודות לפעילות החלבון E2A ולמשוב שלילי של אחד מחלבוני הגן - E4orf4[15]. אולם למרות העיכוב נמשך שעתוק יחידה זו גם בשלבים המאוחרים של ההדבקה.
- E4orf1 - חלבון זה גורם לשפעול האנזים PI3K - אנזים מזרחן, הנחוץ לשפעול האנזים Protein kinase B, המוכר גם בתור PKB .PKB הוא אנזים מזרחן בפני עצמו, אשר גורם לשפעול חלבון mTOR, הנחוץ לשם תרגום החלבונים בתא[16]. על ידי כך מבטיח לעצמו הנגיף את המשך יצור החלבונים הוויראליים הנחוצים לו על מנת להפוך לנגיף בוגר.
- E4orf3 ו-E4orf6 - חלבון E4orf6 נקשר לחלבון E1B-55kDa ואליהם נקשר גם E4orf3. לקומפלקס זה תפקיד חשוב במעבר mRNA של הגנים המאוחרים מהגרעין לציטופלסמה ולשמירה על יציבותו. בנוסף, החלבון E4orf6 נקשר לחלבון p53. כתוצאה מהקישור ביניהם, נמנע האפופטוזה התלוי ב-p53, אשר מושרה על ידי E1A. חלבון E4orf3 נקשר לקומפלקס חלבוני חישת נזקי DNA בתא המאכסן (Mre11-Rad50-Nbs1), שמשתתף בתגובה האנטי-ויראלית, וגורם להיפרדותו[17]. ואילו קישור של E4orf6 לקומפלקס Ubiquitin ligase תאי משרה, יחד עם E1B-55kDa, פירוק של אותם חלבוני חישת נזקי DNA בתא המאכסן לרבות p53 עצמו[18].
- E4orf4 - זהו חלבון קטן במשקל של 14kDa. חלבון זה מעורב במספר תהליכים ויראליים, בהם: בקרה שלילית על ביטוי גנים[19], עידוד תרגום החלבונים הנגיפיים בתא על ידי שפעול ישיר של החלבון mTOR[20], ובקרה על שחבור ה-mRNA הנגיפי המאוחר. כל זאת דרך אינטראקציה ישירה שלו עם הפוספטאז התאי מסוג PP2A[21].
דיכוי המנגנון האנטי-ויראלי בתא
מקטעי ה-VAI-RNA, שגודלם כ-155 בסיסים, אינם מקודדים לשום חלבון ויראלי ועיקר תפקידם הוא לבקר את תהליך השחבור החליפי ותרגום של גנים מוקדמים ומאוחרים וכן לדכא את המנגנון האנטי-ויראלי, שנועד להוריד למינימום את תהליך התרגום של החלבונים בריבוזומים, כמו גם להשרות תגובה אנטי-ויראלית מערכתית של הפרשת ציטוקינים פרו-דלקתיים, דוגמת אינטרפרון.[22] אותו המנגנון האנטי-ויראלי מושתת על האנזים המזרחן Protein kinase R (PKR), אשר מצוי בתאים במצב של מונומר בלתי פעיל. חשיפתו למקטעי RNA דו-גדילי, הנוצרים על פי רוב בעת שכפול הגנום של נגיפי RNA וכן בעת שעתוק גנים נגיפיים (במהלך מחזור ההתרבות של אדנו וירוסים עוברים במקביל חמשת הגנים המוקדמים שעתוק. כיוון שעתוקם שונה בעקבות העובדה כי הם נמצאים על גדילי DNA מנוגדים ולכן באופן רגעי נוצרים מקטעי RNA דו-גדילי המזוהים על ידי חלבון ה-PKR) גורמת לו לעבור הומודימריזציה ואקטיבציה בצורת זרחון עצמי. PKR פעיל מזרחן את פקטור תחילת התרגום eIF2, אשר מתווך את הקישור של tRNA הקשור לחומצת אמינו מתיונין (המסמן את תחילת החלבון) לריבוזום. דבר זה גורם לעצירת תרגום החלבונים בתא.
שלב ביניים


לאחר הסינתזה של חלבוני ה-E2B מתחיל שלב שכפול הגנום. השכפול מתבצע בשיטת ה-Strand displacement[23], כדי לשכפל את שני הגדילים בו זמנית ללא השימוש במקטעי אוקזקי (ראו תרשים מצורף). התהליך מתחיל בניתוק 6 קשרי מימן בקצוות ה-5' של הדו-גדיל ובגיוס קומפלקס חלבוני שכפול, המורכב מחלבונים תאיים ונגיפיים, לאתר התחלת השכפול על ידי חלבון הליבה TP. קומפלקס זה מורכב מהחלבונים הבאים: E2B DNA polymerase, Preterminal protein (pTP), Nuclear factor 1 (NF-1) ו-Octamer transcription factor 1 (Oct-1). אתר תחילת השכפול של הנגיף מכיל רצף של נוקלאוטידי CATCAT בקצוות ה-5' ורצף של נוקלאוטידי GTAGTA בקצוות ה-3'. מיד עם גיוס הקומפלקס החלבוני לאתר תחילת השכפול, מחבר E2B DNA polymerase נוקלאוטיד מסוג ציטידין מונופוספט (dCMP) לחלבון ה-pTP. בשלב זה מתמקם pTP על גבי קצה 3' של ה-DNA הנגיפי, כך שנוקלאוטיד ה-dCMP יוצר קשר מימן עם הגואנין בגדיל הנגדי (1). נוכחות pTP יחד עם dCMP מהווה תחל ל-E2B DNA polymerase, אשר מתחיל לסנתז גדיל חדש מקצה 5' לקצה 3'. במקביל, לגדיל השני נצמדים חלבוני E2A, על מנת להגן עליו בפני אנזימים תאיים שמטרתם לפרק DNA חד-גדילי (2). בתום שכפול גדיל חדש אחד, מתעקל הגדיל השני (זה אשר מצופה בחלבוני E2A) לצורת בועה. צורה זו מתאפשרת הודות ליצירת קשרי מימן בין רצפי ה-CATCAT בקצה 5' לבין רצפי ה-GTAGTA בקצה 3' (3). בתום יצירת קשרי המימן הללו, מגויס קומפלקס חלבוני השכפול פעם נוספת, דבר אשר מוביל לסנתזת הגדיל השני מקצה 5' ל-3', בדומה לגדיל הראשון, ללא שימוש במקטעי אוקזקי (4).
תהליך השכפול הנ"ל אינו מניב DNA נגיפי מוגמר, שכן בגמר השכפול חלק ניכר מהגנום הנגיפי מכיל את החלבון pTP בקצה ה-5' של ה-DNA (5). על מנת שה-DNA הנגיפי יהפוך למוגמר, על חלבוני ה-pTP לעבור חיתוך באמצעות הפרוטאז הנגיפי L3 protease[24]. חיתוך זה מניב את חלבוני ה-TP[25] (6). אולם היות ש-L3 protease מתבטא כחלק מהחלבונים הויראליים המאוחרים, פירוש הדבר הוא שה-DNA הנגיפי עובר "הבשלה" סופית רק בשלב המאוחר של ההדבקה.
שלב זה מתרחש 4-6 שעות לאחר ההדבקה ומוביל לסינתזה של כ-100,000 עותקי DNA אדנו ויראלי חדשים בתא[26].
שלב מאוחר
השלב המאוחר מתחיל כ-20 שעות לאחר ההדבקה ומתאפיין בעיקר בסינתזת חלבונים מבניים (חלבוני קפסיד), לתוכם ייארז הגנום הנגיפי. מאפיין נוסף של השלב המאוחר הוא "הבשלת" הגנום הנגיפי בעקבות סינתזת החלבון L3 protease. מקור כל החלבונים המאוחרים (למעלה מ-40) הוא בגן יחיד, בעל פרומוטר בודד, אשר עובר שחבור חליפי.
שלב זה מתאפיין בהמשך בקרה ויראלית צמודה אחר תהליך התרגום בריבוזומים. בעקבות ביטוי החלבונים המוקדמים E4orf3 ו-E4orf6/E1b55kDa חלה סינתזה יעילה של החלבון הנגיפי המאוחר L4 100kDa. חלבון זה גורם לירידה משמעותית בתרגום mRNA תאי בריבוזומים, בעקבות היעדר זרחון פקטור תחילת התרגום eIF4F[27]. פקטור זה מורכב מקומפלקס של חלבונים: eIF4A - אנזים הליקאז, eI4B - חלבון קופקטור ל-eI4A, eI4E - חלבון מזהה קצה 5' של ה-mRNA (Cap-binding protein) ו-eI4G - חלבון פיגום המזהה את קצה 3' של ה-mRNA (זנב רב-אדנול). החלבון הוויראלי L4 100kDa מנתק את האנזים המזרחן MNK-1 מפקטור eI4F ובכך מונע את זרחון eI4E[28]. היעדר זרחון eI4E גורם כאמור לירידה בתרגום ה-mRNA התאי, שכן על מנת שהתרגום יתרחש על החלבון eI4E להיות מזורחן (ולזהות את ה-"CAP" של ה-mRNA). בהקשר זה חשוב לציין כי גם ה-mRNA הנגיפי מכיל "CAP" בקצה 5', אולם תהליך תרגומו אינו נפגע כתוצאה מהיעדר הזרחון של eI4E. הסיבה לכך היא שימוש במנגנון הוויראלי Ribosome shunting, אשר מאלץ את הריבוזומים בתא לפסוח על ה-"CAP" של ה-mRNA הנגיפי, כלומר להתחיל את התרגום באופן מיידי[29].
בתום השלב המאוחר נארזים הוויריונים הבוגרים לתוך הקפסיד בגרעין התא, עד אשר מגיעים למסה קריטית, דבר הגורם לפיצוץ ממברנת הגרעין ומאוחר יותר לממברנת התא ולשחרור הנגיפים הבוגרים מהתא המאכסן. על פי רוב, מסנתזים נגיפי Adenoviridae כמות גדולה של חלבוני מבנה ביחס לגנומים הויראליים המשוכפלים. עודף של חלבוני מבנה מצטברים בגרעין התא ויוצרים את גופיפי ההסגר (Inclusion bodies), כחלק מהאפקט הציטופתי המושרה על ידי הנגיף בתרבית תאים.
פתוגנזה
מחלות בבני האדם
משפחת ה-Adenoviridae מכילה 5 סוגים של נגיפים, המסוגלים לחולל מגוון רחב של מחלות בקרב בעלי החיים. להלן המחלות להן גורמים זני ה-Mastadenovirus, המדביקים בני אדם[30]:
- דלקות בדרכי הנשימה (דלקת לוע, דלקת גרון, דלקת סימפונונות, דלקת ריאות) - זנים: 1-7, 14, 21 (זנים 1-2, 4-5 ו-7 הם המחוללים השכיחים ביותר).
- דלקת לחמית העין - זנים: 1-4, 6-8, 11, 14, 19, 37 (זנים 3-4, 8 ו-37 הם המחוללים השכיחים ביותר).
- דלקת בדרכי העיכול - זנים: 31, 40-41, 43-47, 52 (זנים 40 ו-41 הם המחוללים השכיחים ביותר).
- דלקת בדרכי השתן (דלקת שלפוחית השתן ודלקת השופכה) ואברי הרבייה (דלקת צוואר הרחם) - זנים: 2, 8, 11, 21, 19, 37 (זנים 11 ו-37 הם המחוללים השכיחים ביותר בהתאמה).
- דלקת קרום המוח ואנצפליטיס - זנים: 7, 12, 32.
- הפטיטיס - זנים: 1-2, 5 (היארעות המחלה נדירה, מתרחשת בעיקר בקרב מושתלי כבד).
- השמנה - במחקר שבוצע בשנת 2005 נטען לראשונה כי נצפה קשר ישיר בין נוכחות נוגדנים ספציפיים כנגד זן 36 לבין השמנה (ב-30% מאנשים הסובלים מהשמנת יתר נמצאו נוגדנים כנגד זן 36), אולם באופן פרדוקסלי נצפתה ירידה ברמת הטריגליצרידים והכולסטרול באותם האנשים[31]. חיזוק נוסף למעורבותו של זן 36 בהשמנה התקבל על סמך מספר מחקרים בהם בוצעה הדבקה מכוונת של חולדות, עכברים, תרנגולות, וקופים בזן 36. הדבקה זו הובילה לעליה משמעותית בהשמנת המינים הנ"ל[32]. מנגנון ההשמנה, בו משתתף הנגיף, טרם הובן סופית, אולם ככל הנראה לחלבון המוקדם E4orf1 תפקיד מרכזי בתהליך[33].
מחלות בכלביים
להלן המחלות להן גורמים זני ה-Mastadenovirus בכלביים:
- הפטיטיס - דלקת כבד זיהומית המלווה באנצפלופתיה כבדית, צהבת, חום גבוה, שיעול, בטן נוקשה ואיבוד תיאבון. מחלה זו נגרמת כתוצאה מהדבקות ב-Canine adenovirus type 1 ועלולה לעיתים לגרום למות החיה[34].
- דלקת בקרנית העין (Canine adenovirus type 1).
- דלקת כלי דם (Canine adenovirus type 1).
- שעלת המכלאות - דלקת בדרכי נשימה העליונות, הנגרמת, בין היתר, כתוצאה מהדבקות ב-Canine adenovirus type 2[35].
מחלות בעופות
להלן המחלות להן גורמים מיני ה-Aviadenovirus, המדביקים עופות:
- דלקות בדרכי הנשימה (דלקת סימפונות - Quail Bronchitis).
- תסמונת ירידה בהטלה (Egg drop syndrome) - הטלת ביצים ירודה, או מנגד הטלת ביצים בעלות גודל, צורה, מרקם וצבע חריגים. המחלה נגרמת כתוצאה מהדבקות ב-Duck adenovirus type 1, השייך לסוג Atadenovirus[36].
- דלקות בדרכי העיכול (Haemorrhagic Enteritis) - דלקת מעיים חריפה המלווה בשלשול דמי.
- הפטיטיס (Inclusion Body Hepatitis) - דלקת כבד זיהומית הנגרמת כתוצאה מהדבקות במיני ה-Fowl adenovirus (Fowl adenovirus type 2 הוא המחולל השכיח ביותר)[37].
- טחול מוגדל (Pheasant Marble Spleen Disease)[38].
- דלקת לבלב.
- דלקת חדרי המוח.
אופן ההידבקות
היות שאתרי המטרה של נגיפי משפחת ה-Adenoviridae הם רבים, קיימות מספר דרכים שבהן ניתן להידבק בנגיפים: דרך הפה על ידי תרסיס באוויר, דרך העיניים על ידי תרסיס אוויר, באמצעות מגע עם נוזל מזוהם בנגיפים (בריכות שחייה שמכילות ריכוז נמוך מהנדרש של כלור), על ידי צריכת מזון או מים נגועים בנגיפים (הדבקה פיקאלית-אוראלית), בדרך אנכית, כלומר מעבר הנגיף מהאם לעובר (Duck Adenovirus A בלבד), וכן דרך קיום יחסי אישות (נגיפי Mastadenovirus אשר גורמים לדלקת במערכת הרבייה). בשנת 2007 בוצע מחקר בו נטען לראשונה כי אמבות מהסוג Acanthamoeba מסוגלות לאכסן את הזנים ההומניים: 1, 2, 8 ו-37. מחקר זה קושר לראשונה בין מחלת ה-Acanthamoeba keratitis - דלקת קרנית אשר נגרמת כתוצאה מהידבקות ב-Acanthamoeba לדלקות בלחמית העין הנגרמות על ידי נוכחות זני הנגיף 8 ו-37. לפיכך תגלית זו מציגה את האמבות כחיות מאגר פוטנציאליות של נגיפי Mastadenovirus[39].
לאחר ההדבקה, הנגיפים דוגרים ומתרבים בגוף במשך פרק זמן של 5-8 ימים. מרבית המחלות הנשימתיות חולפות מעצמן כעבור מספר ימים, אולם חלק מהזנים מוגדרים אלימים יותר מהאחרים (למשל זנים 4 ו-7), ועלולים לגרום למחלות נשימתיות קשות בילדים מתחת לגיל 5. כמו כן, דלקות דרכי העיכול, הנגרמות על ידי זנים 40-41 מצריכות לעיתים קרובות אשפוז בבית חולים.
מניעה
בהיותם נגיפים "ערומים", מפגינים נגיפי Adenoviridae שרידות גבוהה מאוד בתנאי הסביבה. הדבר מאפשר להם להתקיים פרק זמן ממושך יחסית מחוץ לגוף המאכסן (שבוע בטמפרטורה של 36°C, 3-8 שבועות בטמפרטורה של 25°C, למעלה מחודשיים בטמפרטורה של 4°C). שרידות זו מתבטאת בעמידות גבוהה לתנאי יובש, לחות וקרינת UV (יוצא הדופן הוא זן 40, אשר נמצא רגיש לקרינת UV) כמו גם לכימיקלים שונים, לרבות: כהלים, ריכוז נמוך של כלור, בסיסים וחומצות. עם זאת, נגיפי האדנו מגלים רגישות רבה לכימיקלים דוגמת: נתרן תת-כלורי בריכוז של 1%, Sodium dodecyl sulfate בריכוז של 0.25%, גלוטראלדהיד בריכוז 2% ופורמלין. היות שרוב נגיפי Adenoviridae מועברים דרך האוויר על ידי תרסיס, שמירה על היגיינה נאותה, הכוללת שטיפת ידיים קבועה וכיסוי הפה והאף ברגע שיעול ועיטוש, מהווה אמצעי יעיל ביותר לשמירה בפני ההידבקות. שטיפת ירקות ופירות וכן בישול מזון והרתחת המים מהווים מניעה בפני הדבקות בזנים 40-41 (חימום ל-56°C במשך 30 דקות, או מנגד חימום ל-60°C במשך 2 דקות מספיק כדי להרוס את נגיפי האדנו)[40][41].
עבודה עם נגיפי Mastadenovirus נחשבת לבעלת סיכון ביולוגי ברמה 2 (Biosafety level 2).
אבחנה
כיום נהוג להשתמש במספר שיטות לזיהוי הנגיף, הן סרולוגיות והן שיטות של וירולוגיה קלאסית.

- בידוד הנגיף בתרבית - בשיטה זו מדגירים כיח מהגרון על שורת תאים סרטניים כגון HEP2 או HeLa, לקבלת אפקט ציטופתי ייחודי של התעגלות והתנפחות, אשר ירמוז על נוכחות הנגיף בתרבית. החיסרון המרכזי בשיטה זו הוא פרק הזמן הממושך אשר לוקח לתרבית התאים לבטא את האפקט הציטופתי (עד שבוע מרגע הדבקת התרבית). עם זאת יש לציין כי לא ניתן לגדל את הזנים 40, 41 בתרבית תאים.
- אימונופלואורסצנציה ישירה - בשיטה זו מדגירים נוגדנים מונוקלונליים כנגד חלבוני ה-Fiber הנושאים מולקולה פלואורסצנטית (לרוב מסוג FITC). לאחר בדיקה תחת מיקרוסקופ אולטרה סגול, ניתן לאשר או לשלול נוכחות אדנו ויראלית. היתרון המשמעותי של השיטה הזו על פני הקודמת נעוץ במהירות הבדיקה (תוצאות ניתן לראות כעבור שעה). זוהי השיטה המועדפת מבחינת אבחון הנגיף במעבדות הקליניות במסגרת בתי החולים.
- אימונוכרומטוגרפיה - בשיטה זו מטפטפים דוגמה מצואת החולה ישירות על גבי משטח הבדיקה, אשר מצופה בנוגדנים ספציפיים כנגד הזנים 40 ו-41, אשר גורמים כאמור לדלקות בדרכי העיכול. במידה ונוצרת אינטראקציה בין הנוגדנים והנגיפים בדוגמה, מופיע פס צבע כתשובה חיובית. היתרון המרכזי בשיטה נעוץ אף הוא במהירות הבדיקה (תוצאות ניתן לראות כעבור 10 דקות)[42].
- שיטת EIA (קיצור של: Enzyme immunoassay on antigen) - בשיטה זו חרוזים מצופים בנוגדנים מונוקלונליים כנגד חלבוני ה-Fiber מגיבים עם כיח מהחולה. במידה שיש נוכחות נגיף בכיח יתקבל ביטוי צבע שנמדד מאוחר יותר לבליעת אורך גל של האור. היתרון המרכזי של השיטה, פרט למהירות היחסית בה מתבצעת הבדיקה (כחצי שעה), היא היכולת לזהות בין מיני הנגיף השונים ולאבחן כמויות קטנות מאוד של נגיף בכיח (10ng - 50ng בלבד).
- PCR - הגברת רצף DNA ייחודי לנגיף. היתרון של השיטה, על אף היותה יחסית מורכבת ויקרה, היא הקטנת האפשרות לקבלת טעויות בזיהוי הנגיף העלולות להתקבל בשיטות האבחון לעיל (כלומר מניעת False Negative או False Positive).
בהקשר האבחנתי חשוב לציין, שהיות ונגיפי האדנו עלולים להישאר בגוף גם לאחר היעלמות סימני המחלה, אבחנה חיובית לעיתים אינה משקפת את המצב הבריאותי של הפרט.
טיפול וחיסון
כיום לא קיים טיפול תרופתי נגד נגיפים במשפחת Adenoviridae. עיקר הטיפול הרפואי מתבסס על טיפול תומך בסימפטומים הנלווים, דוגמת הורדת חום ושיכוך כאבים.
בעבר פותח חיסון נגד הזנים 4 ו-7 של הסוג Mastadenovirus, הנחשבים לאלימים ביותר לבני האדם[43] (מחוללי מחלות בדרכי הנשימה). החיסון ניתן לחיילי ארצות הברית בין השנים 1971–1999[44], אולם הופסק כאשר החברה שסיפקה חיסונים אלה הפסיקה את ייצורם. ב-16 במרץ 2011 אושר מתן החיסון זה, שפותח מחדש בהתבסס על החיסון המקורי משנת 1971, על ידי טבע תעשיות פרמצבטיות[45].
לנגיפי Adenoviridae מהסוג Aviadenovirus מצויים כיום שני חיסונים זמינים: חיסון על בסיס וירוס מוחלש וחיסון על בסיס וירוס מומת. חיסונים אלה ניתנים לעופות על מנת למנוע תחלואה בתסמונת הטלה ירודה ובדלקות של מערכת העיכול.
לזני הנגיף CAdV-1 ו-CAdV-2 מהסוג Mastadenovirus קיים כיום חיסון על בסיס וירוס CAdV-2 מוחלש, הניתן לכלבים במסגרת חיסון ה-DA2PPC.
ניצול למטרות מחקר

היות שרצפטורי ה-CAR, אותם מנצלים נגיפי משפחת ה-Adenoviridae על מנת לחדור לתוך תאי האפיתל בגוף, מצויים על מגוון רחב של תאים בגוף, עולה פוטנציאל החדירה של נגיפי האדנו. עובדה זו מנוצלת על ידי חוקרים רבים על מנת להשתמש בנגיפי המשפחה (לרוב בזן 5 בסוג Mastadenovirus) לשם החדרת פלסמידים סינתטיים, המבטאים גנים שונים, כשיטת טרנספקציה מקובלת ובמסגרת ריפוי גני[46].
מיון
משפחת ה-Adenoviridae מתחלקת ל-5 סוגים. לכל סוג קיימת קבוצת פונדקאים טיפוסית, אותה הוא מדביק [47][48].
מינים וזנים לא מסווגים בסוג Atadenovirus
מינים לא מסווגים בסוג Aviadenovirus
|
מינים וזנים לא מסווגים בסוג Mastadenovirus
|
מינים וזנים לא מסווגים בסוג Siadenovirus
|
לקריאה נוספת
- David O.White, Frank J. Fenner, Medical Virology fourth edition, 1994. מסת"ב 0-12-746642-8
קישורים חיצוניים
- Adenoviridae, באתר NCBI (באנגלית)
- Adenoviridae, באתר האנציקלופדיה של החיים (באנגלית)
- Adenoviridae, באתר GBIF (באנגלית)
- Adenoviridae, באתר אנציקלופדיה בריטניקה (באנגלית)
- נגיפי Adenoviridae באתר ViralZone
- סרטון של חברת Abnova המדגים עבודה עם נגיפי Adenoviridae הומאניים במעבדה
הערות שוליים
- ↑ נְגִיף אָדֵנוֹ במילון רפואה (תשנ"ט), באתר האקדמיה ללשון העברית
- ↑ Shenk T., Fields BN., Knipe DM., Howeley PM et al. (1996). "Fields Virology Vol. 2". Lippincott-Raven Publishers Philadelphia, pp. 2111-2148.
- ↑ Hearing et al. (2011). "Adenovirus Core Protein VII Protects the Viral Genome from a DNA Damage Response at Early Times after Infection". Journal of Virology 85(9):4135-42. PMID 21345950
- ↑ Bergelson, Droguett, Horwitz and Finberg. (1997). "Isolation of a common receptor for Coxsackie B viruses and adenoviruses 2 and 5". Science 275(5304):1320-3. PMID 9036860
- ↑ Meier and Greber. (2004). "Adenovirus endocytosis". Journal of General Medicine 6 Suppl 1:S152-63. PMID 14978758
- ↑ Leonard and Sen. (1996). "Effects of adenovirus E1A protein on interferon-signaling". Virology 224(1):25-33. PMID 8862396
- ↑ Bandara and La Thanque. (1991). "Adenovirus E1a prevents the retinoblastoma gene product from complexing with a cellular transcription factor". Nature 351(6326):494-7:S152-63. PMID 1710781
- ↑ Shenk and Flint. (1991). "Transcriptional and transforming activities of the adenovirus E1A proteins". Advances in Cancer Research 57:47-85. PMID 1835254
- ↑ Cuconati and White. (2002). "Viral homologs of BCL-2: role of apoptosis in the regulation of virus infection". Genes and Development 16(19):2465-78. PMID 12368257
- ↑ Dobner and Kzhyshkowska. (2001). "Nuclear export of adenovirus RNA". Current Topics in Microbiology and Immunology. PMID 11417126
- ↑ Shenk T., Fields BN., Knipe DM., Howeley PM et al. (1996). "Fields Virology Vol. 2.". Lippincott-Raven Publishers: Philadelphia, pp. 2111-2148
- ↑ Fessler at al. (2004). "Mechanisms of E3 modulation of immune and inflammatory responses". Current Topics in Microbiology and Immunology. 273:113-35 PMID 14674600
- ↑ Lichtenstein and Wold. (2004). "Functions and mechanisms of action of the adenovirus E3 proteins". International Reviews of Immunology. 23(1-2):75-111. PMID 14690856
- ↑ Shenk et al. (1988). "cAMP acts in synergy with E1A protein to activate transcription of the adenovirus early genes E4 and E1A". Genes and Development 2(12A):1517-28. PMID 2850966
- ↑ Bondesson and Akusjarvi. (1996). "Adenovirus E4 open reading frame 4 protein autoregulates E4 transcription by inhibiting E1A transactivation of the E4 promoter". Journal of Virology 70(6):3844-51. PMID 8648720
- ↑ O'Shea et al. (2005). "Adenovirus Overrides Cellular Checkpoints for Protein Translation". Cell Cycle 4(7):883-8. PMID 15970698
- ↑ Hearing et al. (2004). "Relocalization of the Mre11-Rad50-Nbs1 Complex by the Adenovirus E4 ORF3 Protein Is Required for Viral Replication". Journal of Virology 79(10):6207-15. PMID 15858005
- ↑ Stracker et al. (2002). "Adenovirus oncoproteins inactivate the Mre11-Rad50-NBS1 DNA repair complex". Nature 418(6895):348-52. PMID 12124628
- ↑ shenk et al. (1992). "Adenovirus E4orf4 Protein Reduces Phosphorylation of c-Fos and E1A Proteins While Simultaneously Reducing the Level of AP-1". Journal of Virology 66(10):5867-78. PMID 1326648
- ↑ O'Shea et al. (2005). "Adenovirus Overrides Cellular Checkpoints for Protein Translation". Cell Cycle 4(7):883-8. PMID 15970698
- ↑ Shenck et al. (1993). "Adenovirus E4orf4 protein binds to protein phosphatase 2A, and the complex down regulates E1A-enhanced junB transcription". Journal of Virology 67(12):7556-60. PMID 8230475
- ↑ Ghadge and Thimmapaya. (1994). "In vitro analysis of virus-associated RNA I (VAI RNA): inhibition of the double-stranded RNA-activated protein kinase PKR by VAI RNA mutants correlates with the in vivo phenotype and the structural integrity of the central domain". Journal of Virology 68(7):4137-51. PMID 7911532 .
- ↑ Liu, Naismith and Hay. (2003). "Adenovirus DNA replication". Current Topics in Microbiology and Immunology 272:131-64. PMID 12747549
- ↑ Yeh-Kai et al. (1983). "Genetic identification of an endoproteinase encoded by the adenovirus genomen". Journal of Molecular Biology 167(1):217-22. PMID 6306252 .
- ↑ Hay et al. (1997). "Role of preterminal protein processing in adenovirus replication". Journal of Virology 71(9):6381-9. PMID 9261355 .
- ↑ Weitzman and Ornelles. (2005). "Inactivating intracellular antiviral responses during adenovirus infection". Oncogene 24(52):7686-96. PMID 16299529.
- ↑ Schneider et al. (1991). "Adenovirus inhibition of cellular protein synthesis involves inactivation of cap-binding protein". Cell 65(2):271-80. PMID 1849798
- ↑ Cuesta and Schneider. (2000). "Adenovirus-specific translation by displacement of kinase Mnk1 from cap-initiation complex eIF4F". The EMBO Journal 19(13):3465-74. PMID 10880459
- ↑ Schneider and Mohr. (2003). "Translation initiation and viral tricks". Trends in Biochemical Sciences 28(3):130-6. PMID 12633992
- ↑ David O.White, Frank J. Fenner, "Medical Virology fourth edition", (1994). Academic Press, Inc. San Diego, California p. 311.
- ↑ Dhurandhar et al. (2007). "Human adenovirus-36 is associated with increased body weight and paradoxical reduction of serum lipids." International Journal of Obesity. 29(3):281-6. PMID 15611785
- ↑ Atkinson et al. (2005). "Viruses as an etiology of obesity." Mayo Clinic Proceedings. Mayo Clinic. 82(10):1192-8. PMID 17908526
- ↑ Dhurandhar et al. (2008). "Human adenovirus Ad-36 induces adipogenesis via its E4 orf-1 gene." International Journal of Obesity. 32(3):397-406. PMID 17984979
- ↑ Decaro, Martella and Buonavoglia. (2008). "Canine adenoviruses and herpesvirus." The Veterinary Clinics of North America. Small Animal Practice. 38(4):799-814. PMID 18501279
- ↑ Martella and Buonavoglia. (2007). "Canine respiratory viruses". Veterinary Research. 38(2):355-73. PMID 17296161
- ↑ מתוך עלון המידע אודות תסמונת ירידה בהטלה של The Center for Food Security and Public Health (28 במרץ 2006): "http://www.cfsph.iastate.edu/Factsheets/pdfs/egg_drop_syndrome.pdf".
- ↑ Imai et al. (2011). "Inclusion body hepatitis caused by fowl adenovirus in broiler chickens in Japan, 2009-2010". Avian Diseases 55(4):719-23. PMID 22313000
- ↑ Daniels and IItis. (1977). "Adenovirus of ring-necked pheasants: purification and partial characterization of marble spleen disease virus". Infection and Immunity 16(2):701-5. PMID 193796
- ↑ Valladares et al. (2007). "Detection of Four Adenovirus Serotypes within Water-Isolated Strains of Acanthamoeba in the Canary Islands, Spain". Tropical Medicine and Hygiene 77(4):753-6. PMID 17978083
- ↑ מתוך גיליון בטיחות חומרים אודות זני Mastadenovirus: 1, 2, 3, 4, 5 ו-7 של Public Health Agency of Canada: "http://www.phac-aspc.gc.ca/lab-bio/res/psds-ftss/msds3e-eng.php"
- ↑ מתוך גיליון בטיחות חומרים אודות זני Mastadenovirus: 40, 41 של Public Health Agency of Canada: "http://www.phac-aspc.gc.ca/lab-bio/res/psds-ftss/adenovirus-eng.php"
- ↑ הנתונים נכונים עבור ערכת אימונוכרומטוגרפיה מהירה לאיתור Rotavirus ואדנו וירוס (RIDA Quick Rotavirus/Adenovirus Combi - N1003) של חברת r-biopharm: "http://www.r-biopharm.com/product_site.php?product_id=68&product_class_one=QW50aWdlbiBEZXRlY3Rpb24=&product_class_two=VmlydXNlcw==&product_class_three=&product_class_four=&product_range=Food%20and%20Feed%20Analysis&PHPSESSID=e834f512871716dd749d086730076456
- ↑ Centers for Disease Control and Prevention (CDC) (July 2001). "Two fatal cases of adenovirus-related illness in previously healthy young adults--Illinois, 2000". Morbidity and mortality weekly report 50(26):553-5. PMID 11456329
- ↑ Russell et al. (2006). "Vaccine-preventable adenoviral respiratory illness in US military recruits, 1999–2004". Vaccine 24(15):2835-42. PMID 16480793
- ↑ מכתב אישור רשמי ממנהל המזון והתרופות האמריקאי אודות מתן החיסון (16 במרץ 2011): "http://www.fda.gov/BiologicsBloodVaccines/Vaccines/approvedProducts/ucm247511.htm".
- ↑ Hunt et al. (2001). "Adenoviral Gene Therapy". The Oncologist 7(1):46-59. PMID 11854546
- ↑ מבוסס על המאגר הטקסונומי של NCBI: "http://www.ncbi.nlm.nih.gov/Taxonomy/Browser/wwwtax.cgi?id=10508
- ↑ מבוסס על המאגר הטקסונומי של UniProt: "http://www.uniprot.org/browse/uniprot/by/taxonomy/?query=adenoviridae
הבהרה: המידע במכלול נועד להעשרה בלבד ואינו מהווה יעוץ רפואי.
Adenoviridae33729441Q193447

