כולרה
 | |
| צילום במיקרוסקופ אלקטרוני של החיידק Vibrio cholerae, הגורם למחלת הכולרה | |
| שכיחות | 3–5 מיליון מקרים בשנה |
|---|---|
| סיבות | החיידק Vibrio cholerae |
| תסמינים | שלשולים מרובים והתייבשות מהירה |
| אבחון | תרבית צואה ותבחיני אנטיגן |
| טיפול | החזרי נוזלים ומלחים, אנטיביוטיקה |
| מניעה | טיהור מים, חיסון |
| פרוגנוזה | שיעור תמותה של 100,000 בני אדם בשנה |
| קישורים ומאגרי מידע | |
| eMedicine | article/962643 |
| DiseasesDB | 29089 |
| MeSH | D002771 |
| MedlinePlus | 000303 |
| סיווגים | |
| ICD-10 | A00 |
כוֹלֵרָה (בספרות העברית[1] מצוי גם הכתיב חֳלִירַע ובכתיב מלא חולירע; בלועזית: Cholera) היא מחלה זיהומית מידבקת, הנגרמת מהחיידק Vibrio cholerae ומתבטאת בשלשולים מרובים, לעיתים עד כדי התייבשות ומוות. תפוצתה העולמית של המחלה גבוהה, במיוחד באזורים בעלי תשתית תברואה ירודה או אזורים מוכי אסון, ומגיעה לממדי מגפה. החיידק פוגע במערכת העיכול וגורם לאיבוד מהיר של עד ליטר נוזלים בשעה. 50% מהמפתחים מחלה קשה, אם אינם מטופלים, מתים מהמחלה (אך אחוזי התמותה נמוכים יותר).
מקור המילה "כולרה" הוא במונח היווני-לטיני למרה, הליחה הצהובה אשר נקשרה במחלות שלשולים ובעונת הקיץ, בדומה למחלת הכולרה.
אפידמיולוגיה
החולירע בטבריה 1912
|
|---|
|
תיאורים ראשונים של מחלה בעלת מאפיינים של כולרה מופיעים בכתבים עתיקים בסנסקריט, והסברה הרווחת היא כי כולרה הייתה מצויה באזורי הדלתה של נהר הגנגס בהודו במשך מאות בשנים, לאחר שהתפתחה שם בעקבות זיהום הנהר.[2] גרסיה דה אורטה, רופא פורטוגלי ממוצא יהודי שפעל בגואה במאה ה-16, היה הראשון לתאר בפירוט את תסמיני המחלה בספרו, "שיחות על אודות צמחי מרפא וסמים של הודו".
מגפות והתפרצויות
במאות האחרונות התפשטה המחלה לאורך נתיבי סחר ימיים ויבשתיים מחוץ להודו, עם מספר התפרצויות של מגפות כולרה עצומות ממדים במקומות שונים בעולם. מן המאה ה-19 ועד לעשור השני של המאה ה-21 מונים שבע מגפות עולמיות של כולרה, שמקורן בתת-יבשת ההודית, בנוסף למספר התפרצויות מקומיות. עוד לפני כן מתועד כי במאה ה-17 הגיעה המחלה לאינדונזיה, שם תוארה ב-1628 על ידי הרופא ההולנדי יעקובוס בונטיוס, ולפי מקורות סיניים, הגיעה כולרה מהודו לסין ב-1669.
בין השנים 1817–1824 התפרצה מגפת הכולרה הראשונה באזורי סרי לנקה, מאוריציוס, חופי מזרח אפריקה, סין ויפן. דרך ארצות ערב הגיעה המחלה לפרס וסוריה ועד לאימפריה הרוסית. מעריכים כי המחלה התפשטה אל מחוץ לתת-היבשת ההודית דרך חיילים בריטים שלחמו בצפון הודו. מגפת הכולרה השנייה שהגיעה לממדי ענק נמשכה מ-1828 עד 1851 ועברה דרך סין, רוסיה ואירופה, אל האוקיינוס האטלנטי והתפשטה לצפון אמריקה. במגפה זו הוכח שהמחלה מסוגלת להתפשט בארצות בעלות אקלימים שונים ביותר, מהודו הטרופית ועד רוסיה, נורווגיה וקנדה בצפון.
מגפת הכולרה השלישית (אנ'), בין השנים 1846–1863, חבקה גם את כל האזורים הצפוניים של אירופה ואמריקה. רוסיה ספגה את המגפה השלישית באופן הקשה ביותר, כשהמגפה גובה את חייהם של כמיליון בני אדם.[2] התפתחות מסילות הברזל וספינות הקיטור אפשרה את התפשטות המגפה השלישית במהירות גדולה בהרבה מן הראשונה. בהתפרצות שפקדה את לונדון ב-1854 נפגעו קשות תושבי בתים ששתו ממי באר נגועה, ואילו אלה שלא שתו ממנה כמעט שלא נפגעו. הרופא ג'ון סנואו הצליח לשחזר את נתיב התפשטות המחלה, לאתר את הבאר הנגועה ולנטרלה. באמצעות מפה שהמחישה את מעגל התפשטות המגפה על ידי ספירת מקרי המוות ומרחקם מהבאר הצליח סנואו לשכנע כי המחלה מועברת על ידי מים מזוהמים.
מגפת הכולרה הרביעית (אנ') נמשכה מ-1865 עד 1875. לקראת סוף המאה ה-19 נודעה לשמצה ההתפרצות הגדולה בהמבורג שבאה בעקבות מגפה ברוסיה.
מגפות הכולרה הגדולות במאה ה-19 עשו רושם עצום על תושבי אירופה והטילו פחד שכמותו לא נודע מימי "המוות השחור" (מגפת הדבר) במאה ה-14. כשהגיעה המגפה לפריז ב-1832 ברחו רבבות אנשים מן העיר. העיירות היהודיות במזרח אירופה, שבהם עשתה המגפה השמות, זועזעו עמוקות. קהילות הגיעו לסף כיליון, המון פליטים נפחדים נדדו בדרכים. בהרבה מקומות נערכו תהלוכות שכללו נשיאת ספרי תורה לשם עצירת המגפה. גם בכפרים הרוסיים נערכו תהלוכות דתיות של נושאי צלב, שבמהלכן התוו מעגלי כישוף סביב לכפר. ההמונים האשימו את הרופאים ה"כופרים" באסון ואף רצחו כמה מהם.
במאה ה-20 שבה והתפרצה המגפה באירופה, נאפולי (1910-1911),[3] ובאופן מצומצם בקרב הצבאות הלוחמים ובין הפליטים במלחמת הבלקן ב-1913, וכן במחנות שבויים במלחמת העולם הראשונה.
מצרים הייתה מוקד של התפרצויות כולרה בגלל העלייה לרגל למכה, שכן עולי רגל ממצרים היו נפגשים במכה עם עולי רגל מהודו ומן המזרח הרחוק, ולאחר מכן חוזרים למצרים. ב-1902 פרצה מגפה גדולה במצרים והתפשטה משם לטורקיה ולארץ ישראל, בה פגעה המגפה קשה: כ-20,000 איש נספו ומוקדיה העיקרים היו: עזה, לוד והקהילה הערבית ביפו.[4]
ב-1947 הייתה התפרצות זעירה של המחלה במצרים. הודו והמזרח הרחוק נשארו נגועים בכולרה בקנה מידה רחב עד לדור האחרון. מ-1923 עד 1939 מתו כשני מיליון וחצי איש מן המחלה[דרוש מקור]. התפרצות הכולרה של תחילת המאה ה-20, שנחשבת למגפת הכולרה השישית, כמעט ולא הגיעה לאירופה בזכות העלייה באיכות הרפואה הציבורית.[2]
התפרצות המחלה בשנות ה-60, שנחשבת למגפת הכולרה השביעית (אנ'), החלה בשנת 1961 באינדונזיה,[2] והתפשטה לרוב חלקי אסיה עד שנת 1966. התפרצות זו הייתה מזוהה בעבר עם התפרצויות נוספות שהיו בשנות ה-90 באפריקה ובאמריקה הלטינית, אך מחקרים מאוחרים הראו שככל הנראה מדובר בהתפתחות נוספת של המחלה שהתפתחה במקביל להתפרצות הגדולה של שנות ה-60.[5]
ההתפרצות האחרונה שאירעה בארץ ישראל, החלה ב-1 בספטמבר 1970 ונמשכה עד מחצית אוקטובר. בימינו התפרצויות המחלה הן נדירות במערב (המפותח מבחינה סניטארית), אך עדיין מופיעות בכ-40 מדינות ברחבי העולם, בעיקר באפריקה, באסיה ובדרום אמריקה.
בעידן המודרני מתרחשות התפרצויות של כולרה בעיקר באזורים בהם נפגעו תשתיות עקב אסון טבע או מצב מלחמה מתמשך. ב-2010, לאחר רעידת אדמה שהביאה להרס רב, החלה התפרצות של מגפת הכולרה בהאיטי, שהביאה למות אלפים. בשנת 2014, קבע האו"ם כי המגפה גרמה למותם של כ-8,000 איש עד עת פרסום הדו"ח, וכי מדובר בהתפרצות מגפת הכולרה החמורה ביותר בעולם. ב־2017 דווח על התפרצות קשה של מחלת הכולרה בתימן, למעלה מ-125,000 נפגעים, וכאלף הרוגים, על רקע מלחמת אזרחים מתמשכת.[6]
מאפיינים אפידמיולוגיים נוספים
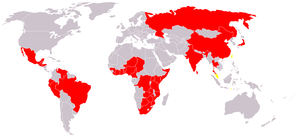
שיעורי התחלואה בכולרה אינם מדויקים מאחר שמקרים רבים מתרחשים במדינות מתפתחות, שם אבחנה ודאית אינה אפשרית, מערכות הדיווח לוקות בחסר ולעיתים ישנו אינטרס של המדינה לטשטש את ממדי המחלה בתחומה בשל השפעת הסטיגמה שיש למחלה על מסחר ותיירות. עם זאת, ארגון הבריאות העולמי אומד את שיעור ההיארעות ב-3–5 מיליון מקרים בשנה.[7]
באירועי מגפה, שיעורי התחלואה אינם משתנים עם הגיל, אם כי מבוגרים מפתחים פחות תסמינים מילדים. במדינות בהן המחלה היא אנדמית, התחלואה גבוהה יותר בקרב ילדים קטנים. יוצאים מכלל זה הם תינוקות יונקים, שנחשפים פחות למים מזוהמים וכן מקבלים נוגדנים בחלב האם.[7]
מזג האוויר וגורמים סביבתיים משפיעים אף הם על מועדי התפרצויות כולרה. במדינות בהן המחלה אנדמית, ובאסיה בפרט, עולה מספר מקרי כולרה לפני עונת גשמי המונסון ואחריה, ובעת שיטפונות עולים שיעורי כולרה בהשוואה לתקופות יבשות. כמו כן, שינויים בטמפרטורת פני המים ושגשוגם של פלנקטון מביאים לגידול באוכלוסיית החיידק.[8]
גורם
 ערך מורחב – Vibrio cholerae
ערך מורחב – Vibrio cholerae

מחולל הכולרה הוא החיידק Vibrio cholerae, מתג גראם-שלילי אווירני בעל צורת פסיק, החי בסביבה מימית ונפוץ באזורי שפך נהר וחוף. החיידק התגלה באופן בלתי תלוי על ידי פיליפו פצ'יני ב-1854 באיטליה, ועל ידי רוברט קוך שלושים שנה לאחר מכן, עת בודד את החיידק בתרבית מצואה נגועה בעת התפרצות במצרים ובהודו.[8]
אורכו של החיידק 1.5–2 מיקרון ורוחבו 0.5 מיקרון. הוא בעל שוטון דק המקנה לו כושר תנועה גבוה, והוא צומח על מצעים פשוטים כגון מי פפטון. הטמפרטורה המיטבית להתפתחותו היא בין 30 ל-40 מעלות צלזיוס, אם כי החיידק מסוגל להתקיים על פני טווח טמפרטורות גדול. החיידק מומת במהירות יחסית במים מזוקקים, וכן מתקשה להתקיים בתנאי יובש, אך במי שתייה, מי ביוב, בהפרשותיו של אדם חולה ובבגדים רטובים הוא יכול להתקיים מספר ימים. באדם נגוע בכולרה, מספרם של חיידקים אלה מגיע לכ-500 מיליון בכל סמ"ק של נוזל מעי.
החיידק מסווג למעל 200 זנים הנבדלים סרולוגית, בהתבסס על האנטיגן O של הליפופוליסכריד. מתוך אלה רק הזנים O1 ו-O139 הם הזנים הגורמים להתפרצויות ולמגפות. הזן O1 נחלק לשני תת-זנים: הקלאסי ואל טור. המגפות המודרניות של כולרה נגרמו כולן, ככל הנראה, מהתת-זן הקלאסי של O1, למעט השביעית המשויכת לאל טור. הזן O139 מוגבל לדרום אסיה.[8]
פתוגנזה
העברה
לרוב, מקור ההדבקה הוא במחזור צואה-פה, עת אדם נגוע המפריש את החיידק בצואתו או במזון או מי שתייה מזוהמים בחיידק. רסיסי צואה הנגועים במחלה יכולים לזהם פירות וירקות המושקים במי ביוב וגם את הידיים, אם אין מקפידים לרחוץ אותן היטב לאחר עשיית הצרכים. לצורך הדבקה נדרש מזרע (אינוקולום) גבוה של 100 מיליון חיידקים, אך פחות מכך אם ישנה ירידה בחומציות הקיבה.[9] תקופת הדגירה של החיידק נמשכת עד חמישה ימים.
החיידק נעלם מהפרשות החולה ימים ספורים (על פי רוב שבוע) לאחר החלמתו. קיים אחוז מזערי של בני אדם, המסוגלים להידבק בחיידק אך לא לחלות במחלה עצמה, הללו הופכים למפרישי-חיידקים, ועלולים להפיץ את המחלה מחוץ לאזור המגפה.
גורמי אלימות ורעלנים
החיידק מגיע לדופן המעי באמצעות שוטון ונצמד אליה בעזרת פילוס המשמש להיצמדות ונקרא toxin coregulated pilus, ובראשי תיבות TCP. הפילי הללו מקודדים בעיקרם על ידי האופרון tcp, שבו הגן tcpA מקודד לתת-יחידה העיקרית בו. אופרון זה נמצא על גבי אי מרענות המקודד למספר גורמי אלימות יחדיו וככל הנראה נרכש בהעברה גנטית אופקית על ידי אב קדמון של החיידק. מעבר להיצמדות עצמה לתאי המעי, הפילוס מתווך יחסי גומלין בין חיידקי הכולרה ליצירת מושבות במעי הדק ומקנה עמידות נגד חומרים במעי שרעילים לחיידק.
בעת התיישבותו במעי החיידק מפריש רעלן מעי (אנטרוטוקסין), שנקרא רעלן הכולרה, הפוגע באפיתל המעי וגורם בתחילה לדלקת, אשר מלווה בפליטה מוגברת של נוזלים (מים ובתוכם מומסים מלחים) מן הגוף אל תוך חלל המעי. רעלן הכולרה הוא חלבון המורכב מתת-יחידות A ו-B. חמש תת-יחידות מסוג B נקשרת לקולטן ספציפי מסוג גליקוספינגוליפיד, GM1, המצוי על פני קרום תא המעי (אנטרוציט). קישור זה מאפשר את חדירתה של תת-יחידה A אל ציטופלזמת התא ופגיעה בו. התת-יחידה A מתווכת את הקישור בין ADP ריבוז לקולטן המצומד לחלבון G אשר מגביר רמות אדנילאט ציקלאז, שגורם לעלייה ברמות cAMP. כתוצאה מכך עולה הפרשת יוני כלור לחלל המעי, עלייה שמלווה באובדן נוזלים לחלל המעי בצורת שלשול.
מקור הגנים המקודדים לרעלן הכולרה, ctxA ו-ctxB, אינו בגנום הקדום של חיידק הכולרה, אלא בבקטריופאג' CTXΦ, אשר הדביק את החיידק והפך אותו לחיידק מחולל מחלה. הקולטן אשר מאפשר את כניסת הבקטריופאג' לתא החיידק הוא TCP, ולא זו בלבד, אחד ממשפעלי השעתוק של הגנים לרעלן הכולרה, דומה גנטית לאופרון tcp ומקודד בתוך אי הפתוגניות של TCP. אחד המנגנונים האמונים על בקרת הפרשת הרעלנים בעת נוכחות החיידק במעי הוא חישת מניין. מנגנוני בקרה נוספים הם משפעלי השעתוק ToxT ו-ToxR, אשר נמצאים בקרום התא החיידקי ומתחילים שרשרת איתותים ביוכימיים אשר מביאים לשעתוקם של גנים הקשורים בגורמי האלימות של החיידק.[10]
תסמינים וסימנים
התסמינים האופייניים למחלה הם הפרשת כמויות גדולות מאוד של שלשול מימי (עד עשרה ליטרים ביום), הקאות, התכווצויות שרירים מלוות בכאב, ירידה בחום הגוף, הלם והפסקת השתן. התמותה במקרים חמורים ובלתי מטופלים מגיעה לכ-50% ולמעלה מזה. סיבת המוות העיקרית היא איבוד נוזלים בעקבות השלשול וההקאה. לרוב המחלה מופיעה באופן פתאומי ללא סימני אזהרה. שרירי הבטן והגפיים מתכווצים בחוזקה, לעיתים עד כדי קריעת שריר. הנשימה נעשית מהירה ושטחית והדופק מהיר וחלש. הקול נחלש והדיבור מתקרב ללחש. בשל ההתייבשות הנוצרת כתוצאה מאיבוד מים, הפנים הופכות כחושות (האף הופך מחודד והעיניים נראות שקועות בארובותיהן) והעור נמלא קמטים. החולה חש צימאון שקשה להרוותו, אולם הכרתו אינה נפגמת. המוות עלול לבוא תוך שעות אך בדרך כלל תוך יומיים לאחר הופעת הסימנים הראשונים.
השינויים הפתולוגיים הם תוצאה של ההפסד העצום של נוזלי גוף ועימם של כלורידים ומתכות אלקליות. קיים גם הפסד ניכר ברמת האשלגן. שיעור הנוזלים בדם יורד, תהליך הגורם לעליית מספר הכדוריות האדומות ביחס לנפח הנוזלים וכן עלייה בריכוז החלבונים בפלסמת הדם. המשקל הסגולי של הדם עולה ולחץ הדם יורד. הפרשת השתן נפסקת וכמות השתנן בדם עולה. לאחר המוות, מופיעה צפידת מוות מהירה, השרירים קשים וצבעם אדום ביותר. גם הכבד והכליות גדושים בדם. המעיים הדקים מתנפחים על ידי נוזלים ולרירית שלהם צבע אדמדם, אך אין הריסה ניכרת של תאי הציפוי ואין בקיעים ברירית. הממצא העיקרי הוא התרחבות רבה של נימים.
סיבת ההפסד העצום של נוזלי הגוף בעקבות מחלת הכולרה עדיין שנויה במחלוקת. יש סבורים, שהוא נגרם על ידי שינויים במעי הגס, המאבד את כושרו לספוג את הנוזלים היורדים לתוכו, ויש סבורים שהוא נגרם על ידי נזק לחומר הרקע הבין נימי והריסת המוצין, על ידי הרעלן החיידקי.
בדיקות עזר
בדיקות דם
למרות שבירת המאזן האלקטרוליטרי במעי, רמות האלקטרוליטים בדם נשמרות על פי רוב, אולם עלייה בקראטינין וב-Blood urea nitrogen יכולה להעיד על התייבשות. ספירת הדם עשויה להדגים המטוקריט גבוה בשל ריכוז הדם על רקע ההתייבשות ולויקוציטוזיס כביטוי למצב הזיהומי החריף. בבדיקת הגזים בדם ניתן לראות חמצת מטבולית עם ערכי pH סביב 7.2, ביקרבונט נמוך בצורה ניכרת עקב יציאתו בשלשולים המרובים ופער אניוני גבוה בשל העלייה בריכוזם של חומצה לקטית, חלבונים וזרחה.
בדיקות מיקרוביולוגיות
ניתן לזהות את חיידק הכולרה בצואה בהסתכלות ישירה דרך מיקרוסקופיית שדה אפל, ולהבחין בין הקבוצות הסרולוגיות באמצעות אנטיסרום. בידוד החיידק וגידולו בתרבית דורשים מצעי מזון בררניים כגון אגר טאורוכלורט-טלורין-ג'לטין (TTG) או אגר תיוסולפט-ציטרט-מלחי מרה-סוכרוז (TCBS). שיטה נוספת לזיהוי במקום של החיידק היא בתבחין מסחרי שבו נעשה שימוש במקלון טבילה בצואה, והוא נועד למקומות שבהם שיטות המעבדה אינן מתקדמות ויש צורך בזיהוי מקורב ומידי.
אבחנה
האבחנה הסופית של כולרה אינה נדרשת בטרם התחלת טיפול, אולם באזורים שאינם אנדמיים גובר הצורך לאבחן באופן ודאי זיהום בכולרה מטעמים אפידמיולוגיים. לפי ארגון הבריאות העולמי החשד לכולרה כגורם למחלה השלשולית מתעורר בהתקיים אחד מאלה:
- באזורים אנדמיים לכולרה, החל מגיל 5, בעת שלשול מימי חריף, בליווי או בהיעדר הקאות
- באזורים שאינם אנדמיים לכולרה, החל מגיל 5, בעת שלשול מימי חריף הגורם להתייבשות חמורה או למוות.
האבחנה מתבצעת כאמור בזיהוי החיידק בדגימות צואה בשיטות המיקרוביולוגיות המצוינות לעיל.
אבחנה מבדלת
באבחנה המבדלת לכולרה עומדות מחלות זיהומיות אחרות של הקיבה והמעיים, לרבות זיהומים הנגרמים כתוצאה מחיידקים אחרים כגון אשריכיה קולי או סלמונלה.
טיפול
נוזלים
עיקר הטיפול בכולרה מתמקד בהשבת מאזן הנוזלים, כאשר אופן מתן הנוזלים וקצב החזר הנוזלים תלויים במידת ההתייבשות, בגיל האדם החולה ובמשקלו. החזר של מים ואלקטרוליטים בשתיית תמיסות השבת נוזלים פומיות (Oral Rehydration Solution, ובראשי תיבות ORS) אפשרי במקרים קלים–בינוניים. תמיסות אלו כוללות מים ואלקטרוליטים כגון נתרן, כלור וגלוקוז, שילוב אשר מגביר את כושר ספיגת הנוזלים חזרה תוך שימוש בנשא גלוקוז מסוג SGLT1, אשר מעביר גלוקוז ונתרן מחלל המעי לתוך תאי הרירית. ניתן להכין תמיסות אלו מתכשירים ייעודיים להכנת ORS או באופן ביתי בהוספת חצי כפית מלח בישול ושש כפיות סוכר לליטר מים נקיים. תמיסות אלה אינן כוללות אשלגן, שאותו ניתן להשיג מהמזון. אנשים שאינם מסוגלים לשתות, ומידת ההתייבשות שלהם אינה דורשת עירוי נוזלים, יכולים לקבל את החזרי הנוזלים בזונדה.
הטיפול באנשים בדרגת התייבשות קשה מכולרה כולל החזרי נוזלים ואלקטרוליטים בעירוי. מבין התמיסות הקיימות, תמיסת הרטמן (לקטט רינגר), ובפרט תמיסת הרטמן בתוספת דקסטרוז בריכוז 5%, היא התמיסה המועדפת להחזר נוזלים בעירוי. תמיסה נוספת בשם סליין כולרה, או תמיסת דאקה, מכילה כבר דקסטרוז, יחד עם יותר אשלגן וביקרבונט מאשר הרטמן, ועל כן היא נותנת מענה לאובדן אלקטרוליטים נוספים בצואה. קצב העירוי הממוצע באדם עם התייבשות קשה הוא 200 מ"ל לק"ג גוף ב-24 השעות הראשונות, כאשר חצי מהכמות ניתנת ב-3–4 השעות הראשונות. לאחר החייאת נוזלים מספקת, וברגע שהאדם המקבל את העירוי מסוגל לשתות, מתווספים גם החזרי נוזלים בשתייה.[8]
טיפול מתאים בנוזלים מפחית את התמותה מכולרה לפחות מ-1%. עם זאת, במדינות נחשלות שבהן תשתית הרפואה ובריאות הציבור ירודה, אנשים רבים מתים מכולרה עוד בטרם מגיעים לטיפול רפואי.
אנטיביוטיקה
התפקיד של אנטיביוטיקה בטיפול בכולרה הוא משני ושמור למקרים בדרגת חומרה בינונית–קשה. הטיפול האנטיביוטי מקצר את משך המחלה, מפחית בכ-50% את נפח השלשולים ומקצר את משך הפצת החיידק לסביבה. מתן האנטיביוטיקה מתבצע רק לאחר תיקון מאזן הנוזלים, על פי רוב לאחר ארבע השעות הראשונות לטיפול בנוזלים. בחירת סוג האנטיביוטיקה מתבססת על דפוסי העמידות המקומיים.
שלוש קבוצות תרופות משמשות בטיפול בכולרה: טטרציקלינים, פלואורוקינולונים ומקרולידים. מבין הטטרציקלינים, טטרציקלין ודוקסיציקלין משמשות בטיפול בכולרה, אולם שיעורי העמידות לקבוצה זו הולכים ועולים, ועל כן הן אינן משמשות לטיפול אמפירי, אלא אם כן ידוע שהתפרצות מסוימת נגרמת מזן הרגיש לתרופה. העמידות למקרולידים נדירה, ועל כן טיפול באזיתרומיצין, אשר ניתן במנה חד-פעמית, הוא המועדף. גם לפלואורוקינולונים דוגמת ציפרופלוקסצין ישנם אזורים עם עמידות נרחבת.
טיפול תומך נוסף
תזונה עתירת קלוריות מיד לאחר החזר הנוזלים הראשוני מומלצת למניעת תת-תזונה וסיבוכי היפוקלמיה והיפוגליקמיה. אמהות מיניקות מעודדות להמשיך להיניק תינוקות חולים במקביל ל-ORS. תוספי אבץ הוכחו כמפחיתים משך שלשולים ונפח צואה בילדים, כמו גם אירועים חוזרים של שלשולים בחודשים שלאחר ההחלמה מכולרה. על כן ממליץ ארגון הבריאות העולמי לתת תוספי אבץ לילדים מתחת לגיל 5.[8]
תרופות עוצרות להפחתת תנועתיות המעיים ותרופות להפחתת הקאות לא הוכחו כמועילות בכולרה, ואף עלולות להאריך את משך הזיהום.
מניעה
 ערך מורחב – חיסון נגד כולרה
ערך מורחב – חיסון נגד כולרה
מגפות הכולרה באירופה במהלך ההיסטוריה נתנו דחיפה עצומה להתפתחות ההיגיינה הציבורית. לאחר המגפות הגדולות, הותקנו מערכות ביוב והונהג סינון דרך חול למי השתייה בערים הגדולות, הוכנסו שיפורים בתנאי הדיור, ובייחוד בבניית בתי שימוש. הארגון התברואתי המודרני הוא במידה רבה תוצאה של הפחד שעוררו מגפות הכולרה הגדולות במאה ה-19.
מערכת סניטרית תקינה (כמו זו שקיימת בארצות מפותחות) היא תנאי הכרחי – ובדרך כלל גם מספיק – למניעת המגפה. היא חסרה עדיין בכמה ערים בהודו ובמזרח הרחוק, ומקרי כולרה מופיעים בהן כמעט מדי שנה. הסגר בזמן מחלה הכרחי, אך אינו מספיק לבדו. מרדכי זאב חבקין פיתח חיסון נגד כולרה על ידי חיידק מומת. השימוש בחיסון הונהג בהודו ובאזורי סיכון אחרים, אך הופסק לימים עקב יעילות נמוכה. בהודו עדיין נוהגים לחסן המונים בזמן מגפה או בזמן סכנת מגפה, ובייחוד עולי רגל למקומות קדושים. לאחר הזריקה מצב החסינות נמשך כ־3–4 חודשים בלבד, זריקות נוספות נדרשות כל שישה חודשים. ב-1995 פותח חיסון חדש הניתן בשתייה, שהוא יעיל ובעל תופעות לוואי מעטות.
גם החלמה מכולרה אינה מבטיחה חסינות מפני מחלה חוזרת. הטיפול המונע הטוב ביותר למחלת הכולרה הוא הקפדה על היגיינה בדגש על שטיפת ידיים, הימנעות ממגע עם צואת החולים, מניעת השקיית ירקות במי ביוב וכן טיהור מי השתייה.
ראו גם
לקריאה נוספת
- Matthew K. Waldor and Edward T. Ryan, Vibrio cholerae, Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases, 8th Edition, Elsevier Saunders, 2015, pp. 2471-2479.
קישורים חיצוניים
- ליטל לוין, היום לפני 39 שנים: מגפת כולרה בישראל, באתר הארץ, 1 בספטמבר 2009
- רוביק רוזנטל, חולירע, לא מה שחשבתם, בלוג השפה העברית של מילון רב-מילים, 28 במאי 2014
 דן בראל, המגפה הנוספת שמאיימת על העולם המתפתח - ולא מעניינת אותו, באתר הארץ, 19 באוקטובר 2014
דן בראל, המגפה הנוספת שמאיימת על העולם המתפתח - ולא מעניינת אותו, באתר הארץ, 19 באוקטובר 2014- יאיר זלטנרייך, לחיות בנאפולי ולמות, מגזין סגולה להיסטוריה וידיעת הארץ, אייר תש"ף, מאי 2020
- כולרה, באתר אנציקלופדיה בריטניקה (באנגלית)
 כולרה, דף שער בספרייה הלאומית
כולרה, דף שער בספרייה הלאומית
הערות שוליים
- ↑ בסוגים של 'עברוּת' מתבטא בצורת - 'חוֹלִי-רַע'
- ^ 2.0 2.1 2.2 2.3 CHOLERA, Austin Community College (ארכיון)
- ↑ McNeill, William Hardy. Naples in the Time of Cholera, 1884-1911. Bulletin of the History of Medicine, vol. 71 no. 3, 1997, p. 546-547. Project MUSE,
- ↑ שפרה שורץ, "קופת-חולים הכללית - עיצובה והתפתחותה כגורם המרכזי בשירותי הבריאות בארץ-ישראל", המרכז למורשת בן-גוריון, קריית שדה-בוקר, הוצאת הספרים של אוניברסיטת בן-גוריון בנגב, 1997, עמוד 12
- ↑ Evolution of Seventh Cholera Pandemic and Origin of 1991 Epidemic, Latin America, CDC
- ↑ סוכנויות הידיעות, התפרצות כולרה בתימן: 8,500 נדבקו, 115 מתו, באתר ynet, 15 במאי 2017
- ^ 7.0 7.1 Sajeev Handa, Cholera, eMedicine, June 22, 2017
- ^ 8.0 8.1 8.2 8.3 8.4 Harris JB, LaRocque RC, Qadri F, Ryan ET, Calderwood SB, Cholera, Lancet. 2012;379(9835):2466
- ↑ Nelson EJ, Harris JB, Morris JG Jr, Calderwood SB, Camilli A, Cholera transmission: the host, pathogen and bacteriophage dynamic, Nat Rev Microbiol. 2009;7(10):693
- ↑ Matson JS, Withey JH, DiRita VJ. Regulatory networks controlling Vibrio cholerae virulence gene expression. Infect Immun. 2007 Dec;75(12):5542-9. doi: 10.1128/IAI.01094-07.
הבהרה: המידע במכלול נועד להעשרה בלבד ואינו מהווה יעוץ רפואי.
כולרה38283479Q12090
