כרצת
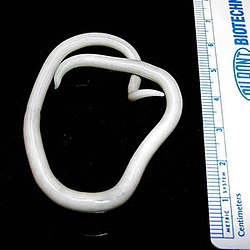 | |
| תולעת כרץ, מחולל המחלה | |
| תחום | מחלות זיהומיות |
|---|---|
| שכיחות | 450 מיליון איש ברחבי העולם (זיהום כרוני) |
| סיבות | התולעת הנימית כרץ |
| תסמינים |
שלב חריף: כאב בטן, בחילה, הקאה שלב כרוני: סימני חסר ויטמין A, חסימת מעיים, תמונה דמוית אסתמה |
| אבחון |
משטח צואה עבה קאטו-כץ לאיתור ביצי התולעת PCR |
| טיפול |
אלבנדזול מבנדאזול |
| מניעה |
שיפור תברואה טיפול המוני |
| קישורים ומאגרי מידע | |
| eMedicine | article/212510 |
| DiseasesDB | 934 |
| OMIM | 604291 |
| סיווגים | |
| ICD-10 | B77 |
| ICD-11 | 1F62 |
כָּרֶצֶת (Ascariasis) היא מחלה זיהומית הנגרמת על ידי התולעת הנימית כרץ (Ascaris lumbricoides). זוהי מחלת התולעים הטפיליות השכיחה בעולם, והיא נפוצה במקומות עם תשתית תברואה ירודה באקלים טרופי וסובטרופי. המחלה נרכשת באופן צואתי-פומי על ידי בליעה של אדמה או מזון הנגועים בביצי התולעת. בשלב החריף של הזיהום, עת פגיות התולעת נודדות בגוף, המחלה יכולה להתבטא בכאבי בטן, בחילות והקאות, כמו גם קוצר נשימה וצפצופים בנשימה, כביטוי לתגובה החיסונית נגד הטפיל. בשלב הכרוני, כתלות בעומס התולעים במעי הדק, עלולות התולעים הבוגרות לגרום לחוסרים תזונתיים, לחסימת מעיים ולתמונה דמוית אסתמה. האבחנה מתבצעת על ידי איתור ביצי התולעת בצואה, או על ידי PCR לזיהוי הביצים בצואה. הטיפול במחלה הוא בתרופות אנטיהלמינתיות, כגון אלבנדזול או מבנדאזול.
אפידמיולוגיה
מחקרים בני ימינו מצביעים על קיומן של ביצי כרץ בקופרוליטים מתקופת הברונזה.[1] במסכת גיטין בתלמוד הבבלי מובאת תרופה לתולעי המעיים ("כירצא").[2]

כרצת היא מחלת התולעים הטפיליות השכיחה בעולם. מעריכים כי 450 מיליון איש נגועים בתולעים באופן כרוני, נכון לשנת 2017, עם כ-600 מקרים חדשים בשנה.[3] ניכר כי ישנה ירידה בשיעור ההימצאות של המחלה, אשר בשנת 2010 תואר כי למעלה ממיליארד איש נגועים בה.[4]
הידבקות במחלה מתרחשת לאורך כל השנה באקלים לח טרופי וסובטרופי, ובאזורים יבשים יותר, כאשר ביצי התולעת יכולות להישאר בנות חיוּת באדמה במשך חודשים, היא מתרחשת כתלות בעונה.[5] הגיל הנפוץ ביותר הוא הילדות המוקדמת.
התמותה נמוכה ונאמדת בכ-2,700 מקרי תמותה בשנה, אולם עומס המחלה גבוה, ובפרט ישנה פגיעה בגדילה והתפתחותם של ילדים.[5]
בישראל מעריכים כי למעלה מ-40% מתושבי הארץ לפני קום המדינה היו נגועים בכרצת בשל דישון היבולים במי ביוב. עם הפיקוח על הגידולים החקלאיים והמעבר לדשנים סינתטיים, ירד אחוז הנגועים לפחות מ-1%.[6]
אטיולוגיה
 ערך מורחב – כרץ
ערך מורחב – כרץ
כרץ (Ascaris lumbricoides) היא תולעת נימית טפילית עגולה ולבנה. בעוד אורכו של הזכר מגיע לכ-30 ס"מ וקוטר רוחבו עד 4 מ"מ, אורכה של הנקבה מגיע עד 50 ס"מ וקוטרה עד 6 מ"מ. ביצי התולעת עמידות לתנאי יובש וטמפרטורות נמוכות, ועל ידי כך יכולות לשרוד באדמה במשך חודשים ושנים.
מין נוסף של כרץ, Ascaris suum, המדביק בעיקר חזירים, תועד גם כגורם לכרצת באדם בקרב אוכלוסיות שלהן מגע קרוב עם חזירים ואדמה המזוהמת בצואת חזירים.[7]

מחזור החיים
הנקבה הבוגרת מטילה במעי המאכסן כ-200 אלף ביצים מדי יום, ואלה מופרשות בצואה אל הקרקע. בעוד שהביצים שאינן מופרות לא זוכות להתפתח, הביצים המופרות מתפתחות לכדי פגיות, אשר בוקעות במעי הדק לאחר אכילתן. משבוקעות הפגיות הן חודרות דרך דופן המעי אל כלי הדם המתנקזים לווריד שער הכבד ומגיעות אל הכבד, שם הן משילות את הקוטיקולה. מהכבד, לאחר כשבוע מבליעת ביצי התולעת,[4] הפגיות נודדות עם זרם הדם אל הריאות. בריאות הפגיות חודרות לחלל הנאדיות וממשיכות לנדוד במעלה עץ הסמפונות וקנה הנשימה לעבר מכסה הגרון, אז הן נבלעות חזרה ומגיעות שוב למעי הדק, כעשרה ימים לאחר תחילת הזיהום. במעי הדק הפגיות הופכות לתולעים בוגרות, שם הן יכולות לחיות במשך שנה עד שנתיים, כשלאחר כחודשיים–שלושה מעת הזיהום התולעים מטילות את ביציהן.[5][7]
העברה
המחלה מועברת במחזור צואה-פה על ידי אכילה של אדמה או של מזון המזוהמים בצואה שבה ביצי כרץ. השקיה של יבולים בביוב גולמי, ולעיתים גם במי קולחין, עלולה לזהם את היבול בביצי כרץ, ועל ידי כך להעביר את המחלה. העברה ישירה בין אדם לאדם אינה אפשרית.
פתוגנזה
השלב החריף
בשלב החריף של הזיהום, שבו פגיות הכרץ נודדות בגוף, הן מפרישות תוצרי פירוק העלולים להשרות תגובת רגישות יתר מסוג I ותגובה חיסונית מסוג 2 עם ייצור מוגבר של נוגדנים מסוג IgE ואאוזינופיליה, עד כדי ביטויים של דלקת ריאות אאוזינופלית, תסמונת לפלר ואסתמה.[5][7]
השלב הכרוני
השלב הכרוני נגרם כתוצאה מהתולעים הבוגרות במעי. התולעים מתחרות על חומרי המזון במעי ועלולות לגרום לאיבוד חלבונים ולמחסור בוויטמין A, כמו גם לאנמיה, שיכולה להיות מוסברת על ידי הדלקת הכוללת במעי ודימום מדרכי העיכול העליונות. התולעים עצמן, הגם שהן עשויות להגן מפני זיהומי מעיים אחרים, משנות את המאזן החיידקי במעי ועלולות לנוע ולגרום לדלקות באתרים שונים במערכת העיכול, כגון התוספתן, כיס המרה, הלבלב והקיבה. בעומס תולעים גבוה, עלול ריבוי התולעים לגרום לחסימת מעיים, או התפשלות מעיים בילדים.[5][7] ילדים קטנים חשופים במיוחד לסיבוך זה נוכח חלל מעי קטן יותר, בפרט באזור הצר של השסתום בין המעי הדק למעי הגס.
כחלק ממנגנוני ההגנה של הכרץ, הוא מפריש מעכבים של אנזימי עיכול ופרוטאזות אחרים שמקורם בתגובה החיסונית. דוגמה לכך היא האנזים מעכב קרבוקסיפפטידאז (ACI), אשר נקשר לאתר הפעיל של מטאלוקרבוקסיפפטידאזות, ובכך חוסם את הביקוע של חלבוני התולעת. באותו אופן מעוכב האנזים טריפסין.
ארגון הבריאות העולמי מסווג את עוצמת הזיהום לפי ריכוז הביצים בצואה: זיהום בעוצמה קלה מוגדר עד 5,000 ביצים לגרם צואה, בעוצמה בינונית עד 50,000 ביצים לגרם צואה, ובעוצמה חמורה מעל 50,000 ביצים לגרם צואה.[8]
תסמינים וסימנים
השלב החריף
השלב החריף, המתאפיין כאמור בנדידת פגיות התולעת בגוף, עשוי להתבטא בכאב בטן, בחילה והקאות כתוצאה מנוכחות הפגיות במעיים ובכבד, וכאשר הפגיות מגיעות לריאות ומעוררות שם דלקת אאוזינופילית חריפה, הדבר עשוי להתבטא בקוצר נשימה, בשיעול עד כדי גניחת דם, בסרפדת ובצפצופים חריפים.[5][7]
השלב הכרוני
רוב מקרי הזיהום הכרוני בכרץ אינם תסמיניים, או לכל היותר מתבטאים בתסמינים קלים של תפיחות בטנית, כאב בטן ובחילה. אך בעת עומס גבוה של כרצים במעיים, הפגיעה בספיגת חומרי המזון עלולה להביא לחוסרים תזונתיים, שיבואו לידי ביטוי בתשישות, חוסר תיאבון ושלשולים. מחסור בוויטמין A עלול לגרום לעיוורון לילה וליובש בעיניים ובעור. החוסרים התזונתיים יכולים בסופו של דבר להביא גם לעיכוב התפתחותי, גופני וקוגניטיבי, שיכול להתבטא, למשל, בירידה בהישגים הלימודיים. העומס הגבוה גם יכול לגרום לחסימה מכנית של המעיים, בפרט בילדים צעירים, אשר מסתמנת כבטן חריפה, ולעיתים דימום מדרכי העיכול העליונות. חדירה של התולעת לדרכי המרה ייתכן שתגרום לצהבת ולחום. התגובה האאוזינופילית לתולעת יכולה להפוך לכרונית עם תמונה דמוית אסתמה של קוצר נשימה התקפי, שיעול וצפצופים.[5][7]
בדיקות עזר
דגימות צואה
בדגימות צואה ניתן להבחין בביצי הכרץ. במשטח צואה בשיטת קאטו-כץ נדגמת כמות ידועה של צואה, 41.7 מ"ג, ותחת מיקרוסקופ אור מתבצע כימות של מספר הביצים, אשר מתוקנן לגרם צואה. ישנו מתאם בין כמות הביצים במשטח לעומס הטפילי של התולעת במעי.[9] שיטות נוספות לספירת ביצים בצואה מאפשרות דגימה של כמות גדולה יותר של צואה, ועל ידי הרחפה, סינון וסרכוז, מגבירות את הרגישות לאיתור הביצים. עם שיטות אלה נמנות שיטת מקמאסטר, שיטת FECPAK ושיטת FLOTAC, המשתמשת במכשיר ייעודי לסרכוז ולהרחפה של הצואה.[10]
נוסף על איתור הביצים תחת מיקרוסקופ, בדיקות PCR על דגימות צואה מאפשרות זיהוי מהיר של נוכחות הביצים בדגימות צואה.[5]
בדיקות נוספות
ספירת הדם מאופיינת על פי רוב באאוזינופיליה. לעיתים ניתן לראות רמת נוגדנים כוללת גבוהה יחד עם כיל גבוה של נוגדנים מסוג IgG4. לנוגדנים נגד הכרץ תגובתיות צולבת עם נוגדנים נגד תולעים טפיליות אחרות, אף שהם יכולים לרמז במידה מסוימת על מידת פעילות המחלה. לא קיימים תבחיני אנטיגן לאיתור כרצת.[9]

דלקת ריאות אאוזינופילית בשלב נדידת הפגיות עשויה להיראות בצילום חזה בצורת תסנינים ריאתיים. בצילום בטן עם בליעת בריום המשמש חומר ניגוד רדיולוגי ניתן לעיתים לראות עומס תולעים גבוה במעיים. בנוסף, גסטרוסקופיה עשויה להדגים בצורה ישירה את התולעים הבוגרות במעי.
אבחנה
משטח קאטו-כץ הוא מדד הזהב לאבחנה של כרצת, בפרט באזורים אנדמיים. יתרונותיה של הבדיקה הם בעלותה הנמוכה ובפשטות הכנתה, סגוליותה גבוהה והיא מעידה על עומס הזיהום ומאפשרת אבחנה של זיהום משולב במספר טפילי מעי. לעומת זאת, רגישות הבדיקה נמוכה, הגם שהיא עולה ככל שמספר הדגימות מאותו אדם עולה, ישנה שונות בין הדגימות מאותו אדם, שכן פיזור הביצים בצואה אינו אחיד, והיא דורשת זמן רב וצוות מעבדה מיומן.
הרגישות והסגוליות של בדיקות PCR, לעומת זאת, גבוהות, וניתן לבצע תבחיני PCR משולבים לאיתור מספר מזהמים. רגישותה הגבוהה של הבדיקה מאפשרת אבחנה של כרצת גם באזורים שבהם העומס הטפילי נמוך. עם זאת, מחירם של תבחיני PCR גבוה יחסית, ועל כן השימוש בהם אינו נפוץ בעולם המתפתח.
לתבחינים סרולוגיים אין מקום של ממש באבחנה של כרצת.
טיפול
הטיפול המקובל לכרצת הוא תרופות ממשפחת הבנזימידאזולים: אלבנדזול במינון 400 מ"ג או מבנדאזול במינון 500 מ"ג, על פי רוב במנה חד-פעמית, אולם בעומס טפילי גבוה ניתן לתת אותן גם במשך מספר ימים.[11] התרופות הללו עובדות במספר מנגנונים על התולעת: הן מעכבות ייצור מיקרוטובולים על ידי קישור לאתר קושר קולכיצין של בטא-טובולין, ובכך גורמות לפגיעה בפילמור דימרים של טובולין בתאי המעי של התולעת. כתוצאה מכך נפגעת יכולת התולעת לקלוט גלוקוז וחומרי מזון אחרים, דבר שמביא בסופו של דבר להרג התולעת. יעילותה של מנה חד פעמית של אלבנדזול או מבנדזול עומדת על כ-90%.[12]
עוד בקו הראשון לטיפול נמצאת גם פיראנטל,[11] שחוסמת את הדה-פולריזציה בצומתי העצב–שריר של התולעת, ועל ידי כך גורמת לכיווץ שריריה ולשיתוקה. גם במקרה זה, מנה אחת מביאה לריפוי בשיעור של כ-90%.[12] תרופות נוספות שמתוארות כבעלות יעילות נגד כרצים הן איברמקטין וניטזוקסניד.[11]
אף שאין התוויה לכך, ניתן לבצע בדיקה חוזרת של דגימות צואה לאיתור ביצים כשבועיים לאחר תילוע, ובדיקה נוספת כחודשיים–שלושה לאחר התילוע על מנת לוודא הכחדה של התולעת. אנשים שבצואתם עדיין נמצאות ביצי כרץ מטופלים בשנית, תוך ניסיון להבין אם מדובר בחשיפה חוזרת או כשל טיפולי.[11]
במקרים של חסימת מעיים נדרש לעיתים ניתוח לכריתת מקטע המעי הנמקי. חדירה של התולעת לדרכי המרה בדרך כלל מטופלת תרופתית, אולם אם הטיפול השמרני נכשל, ERCP עשוי לנקז את המרה ולשלוף את התולעים.[7]
מניעה
שיפור תשתיות התברואה, ובכלל זה טיפול נאות בשפכים וגישה רחבת-היקף למי שתייה נקיים ושירותי רפואה, הוא חלק הכרחי בשבירת שרשרת ההדבקה בכרצת.
ארגון הבריאות העולמי שם לו למטרה להפחית את התחלואה בזיהומי תולעים טפיליות המועברות מן הקרקע, ובכלל זה כרצת. לצורך כך גובשה אסטרטגיה למתן טיפול אנטיהלמינתי המוני תקופתי בתרופות המנויות לעיל לאוכלוסיות בסיכון גבוה ללקות בזיהומים אלה, כגון ילדים בגילאי בית ספר וטרום בית ספר, נשים בגיל הפוריות ומבוגרים העוסקים במקצועות בעלי חשיפה יתרה לזיהומים אלה, דוגמת קוטפי תה וכורים. טיפול זה ניתן פעמיים בשנה באזורים שבהם שכיחות זיהומים אלה גבוהה, קרי אזורים שבהם מעל 50% מהילדים בגילאי בית ספר נגועים, ופעם בשנה באזורים שבהם שכיחות הזיהומים בינונית, קרי אזורים שבהם מעל 20% מהילדים בגילאי בית ספר נגועים.[8] עם זאת, בשל שיעורי הדבקה חוזרת גבוהים, תוכניות אלה אינן מספיקות להפחתה משמעותית של התחלואה בזיהומי תולעים טפיליות.[5]
ראו גם
קישורים חיצוניים
- רונית אפטר, הסיבה לכאבי הבטן שנמשכו עשור: תולעת טפילה באורך 30 סנטימטרים, באתר מעריב אונליין, 19 ביוני 2019
הערות שוליים
- ↑ Barsch E, Kowarik K, Rodler K, Hörweg C, Reschreiter H, Sattmann H, Walochnik J. First molecular data on the human roundworm Ascaris lumbricoides species complex from the Bronze and Iron Age in Hallstatt, Austria. Sci Rep. 2023 Jul 25;13(1):12055. doi: 10.1038/s41598-023-38989-8.
- ↑ תלמוד בבלי, מסכת גיטין, דף ס"ט, עמ' ב'
- ↑ GBD 2017 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2018 Nov 10;392(10159):1789-1858. doi: 10.1016/S0140-6736(18)32279-7.
- ^ 4.0 4.1 Christina Dold, Celia V. Holland, Ascaris and ascariasis, Microbes and Infection, Volume 13, Issue 7, 2011, Pages 632-637, ISSN 1286-4579, https://doi.org/10.1016/j.micinf.2010.09.012.
- ^ 5.0 5.1 5.2 5.3 5.4 5.5 5.6 5.7 5.8 Rojelio Mejia, Jill Weatherhead, Peter J. Hotez, Intestinal Nematodes (Roundworms), Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases, 8th Edition, Elsevier Saunders, 2015, Vol. 2, pp. 3437-3439
- ↑ גדעון ויטנברג"כרץ", האנציקלופדיה העברית (כרך כ, עמ' 1065–1067), חברה להוצאת אנציקלופדיות, תשל"א.
- ^ 7.0 7.1 7.2 7.3 7.4 7.5 7.6 Jourdan PM, Lamberton PHL, Fenwick A, Addiss DG. Soil-transmitted helminth infections. Lancet. 2018 Jan 20;391(10117):252-265. doi: 10.1016/S0140-6736(17)31930-X.
- ^ 8.0 8.1 WHO, Soil-transmitted helminthiases: eliminating soil-transmitted helminthiases as a public health problem in children: progress report 2001-2010 and strategic plan 2011-2020, 2012
- ^ 9.0 9.1 Lamberton, P.H.L., Jourdan, P.M. Human Ascariasis: Diagnostics Update. Curr Trop Med Rep 2, 189–200 (2015). https://doi.org/10.1007/s40475-015-0064-9
- ↑ Marco Albonico et al., Comparison of three copromicroscopic methods to assess albendazole efficacy against soil-transmitted helminth infections in school-aged children on Pemba Island, Transactions of The Royal Society of Tropical Medicine and Hygiene, Volume 107, Issue 8, August 2013, Pages 493–501, https://doi.org/10.1093/trstmh/trt051
- ^ 11.0 11.1 11.2 11.3 Ascaris lumbricoides Infections, in: David W. Kimberlin, Elizabeth D. Barnett, Ruth Lynfield, Mark H. Sawyer (eds.), Red book : 2021-2024 report of the Committee on Infectious Diseases, 2021, American Academy of Pediatrics, 32nd Ed. pp. 210-211
- ^ 12.0 12.1 Keiser J, Utzinger J. Efficacy of Current Drugs Against Soil-Transmitted Helminth Infections: Systematic Review and Meta-analysis. JAMA. 2008;299(16):1937–1948. doi:10.1001/jama.299.16.1937
הבהרה: המידע במכלול נועד להעשרה בלבד ואינו מהווה יעוץ רפואי.
כרצת38282447Q842428
